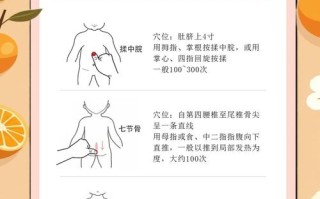
就是妈妈的“免疫系统”把宝宝的“红细胞”当成了“入侵者”并进行攻击。

(图片来源网络,侵删)
以下是导致母婴血型不合,进而引起新生儿溶血的几种主要情况,按重要性排序:
ABO血型不合溶血病
这是最常见的新生儿溶血病类型,约占所有溶血病的60%以上。
-
发生机制:
- 母亲血型为 O型,胎儿血型为 A型或B型。
- O型血的母亲血浆中天然存在抗A和抗B抗体(IgG性质),这些抗体可以通过胎盘屏障进入胎儿血液循环。
- 当这些抗体遇到胎儿的A型或B型红细胞时,就会与之结合,标记其为“敌人”,激活胎儿的免疫系统来破坏这些红细胞,导致溶血。
-
特点:
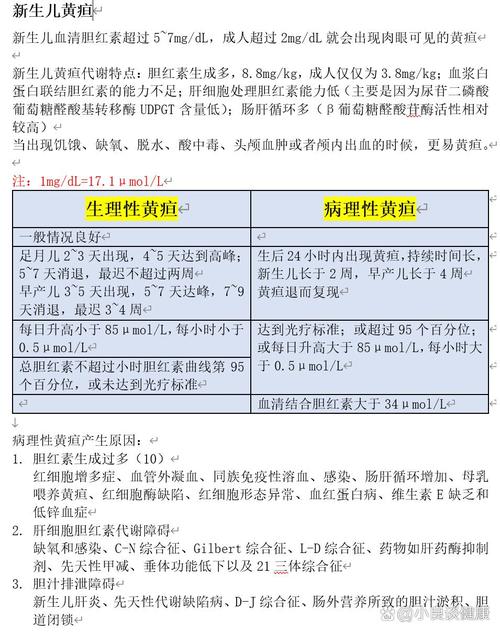 (图片来源网络,侵删)
(图片来源网络,侵删)- 非常常见:但大多数情况下溶血程度较轻,因为胎儿体内的红细胞抗原表达较弱,且肝脏等器官可以处理一部分胆红素。
- 可发生于第一胎:因为母亲体内的抗A/抗B抗体是天然存在的,不是怀孕后才产生的,所以第一胎也可能发生。
- 症状差异大:有的宝宝可能只是轻微黄疸,有的则可能出现严重贫血和高胆红素血症。
Rh血型不合溶血病
这是最严重的新生儿溶血病类型,虽然发病率低于ABO溶血,但后果可能更严重。
-
发生机制:
- 母亲血型为 Rh阴性,胎儿血型为 Rh阳性。
- Rh阴性血的母亲在首次怀Rh阳性的胎儿时,通常不会立即发生溶血,但在分娩过程中,胎儿的Rh阳性红细胞可能会进入母体血液循环,刺激母体产生抗D抗体(这是一种“免疫性抗体”,需要致敏过程)。
- 当这位母亲再次怀上Rh阳性的胎儿时,她体内已有的抗D抗体就会通过胎盘,大量攻击胎儿的Rh阳性红细胞,引发强烈的溶血反应。
-
特点:
- 症状严重:溶血反应强烈,容易导致胎儿重度贫血、心力衰竭、全身水肿(胎儿水肿综合征),甚至死胎或新生儿死亡。
- 很少发生于第一胎:因为需要一次“致敏”过程,但如果在第一胎怀孕期间有流产、羊水穿刺、胎盘早剥等情况,导致母胎出血,也可能在第一胎就发生。
- 可预防:这是目前唯一可以有效预防的新生儿溶血病,通过在母亲分娩(或流产)后72小时内注射抗D免疫球蛋白(Rhogam),可以清除进入母体的胎儿红细胞,阻止母体产生抗D抗体。
其他血型系统不合溶血
除了ABO和Rh系统,还有其他一些血型系统不合也可能引起新生儿溶血,但相对少见。
(图片来源网络,侵删)
- Kell血型系统:是仅次于ABO和Rh的第三大常见原因,母亲的抗-K抗体可以攻击胎儿的红细胞,导致严重的溶血和贫血,但其对红细胞的破坏机制与Rh抗体类似。
- Kidd血型系统:抗-Jk抗体也可能引起溶血,且抗体可能消失后再次出现。
- Duffy、Kidd、Lutheran等血型系统:这些系统的不合也可能导致溶血,但更为罕见。
总结与核心要点
| 血型系统 | 母亲血型 | 胎儿血型 | 发生特点 | 严重程度 | 预防/治疗 |
|---|---|---|---|---|---|
| ABO | O型 | A型或B型 | 最常见,可发生于第一胎,多数较轻 | 多数较轻 | 产后对症治疗(蓝光等) |
| Rh | Rh阴性 | Rh阳性 | 最严重,多发生于第二胎及以后,少数第一胎 | 可非常严重,可致死 | 可预防(产前注射抗D免疫球蛋白) |
| 其他 | 如Kell阴性等 | 如Kell阳性等 | 相对少见 | 不等,部分可很严重 | 产前监测,产后对症治疗 |
如何预防和应对?
-
产前检查至关重要:
- 首次产检:所有孕妇都应进行ABO和Rh血型检测。
- Rh阴性孕妇:必须进行抗体筛查,如果发现抗D抗体或其他抗体,需要密切监测胎儿情况(如B超监测胎儿贫血、羊水胆红素水平等)。
- 预防措施:对于未产生抗体的Rh阴性孕妇,在孕28周左右和产后72小时内各注射一次抗D免疫球蛋白,可有效预防。
-
产后监测:对于有高危因素的孕妇(如O型血、Rh阴性血),新生儿出生后要密切监测黄疸出现的时间、程度和胆红素水平,以便及时发现和治疗。
-
治疗方法:一旦发生新生儿溶血,主要治疗手段包括:
- 蓝光治疗:降低血清胆红素水平,防止胆红素脑病。
- 换血疗法:对于病情严重、胆红素水平极高或已出现贫血的宝宝,这是最有效的治疗方法,可以换出致敏红细胞和抗体,输入正常红细胞。
- 药物治疗:如静脉注射免疫球蛋白,可以阻断抗体对红细胞的破坏。
新生儿溶血病主要由母婴血型不合引起,其中ABO血型不合最常见,而Rh血型不合后果最严重但可预防。规律的产前检查和及时的干预是保障母婴健康的关键。
标签: 母婴血型不合溶血机制 ABO溶血发病原因
版权声明:除非特别标注,否则均为本站原创文章,转载时请以链接形式注明文章出处。